如果您觉得对您有帮助,请帮忙点点上面↑↑↑ “化学一点通” 关注一下公众号
关于硫代硫酸钠中S的化合价问题很多老师咨询。本次给大家做一下分析,请看下列资料:

《普通化学》;(苏)格林卡(Н.Л.Глиика)著;肖涤凡译

《中学化学教与学艺术探究》;马金星,王燕编著



《硫代硫酸根中硫元素的氧化数问题的探讨》作者:韩有月葛秀涛(阜阳师专学报)

《硫代硫酸钠中硫氧化数的实验推证》作者:陈琳(化学教学)
根据上述资料,显然不同的资料对于硫代硫酸或硫代硫酸根中S的化合价是有争议的。有的资料认为中心S为+4价,配位S为0价;有的认为中心硫+6价,配位S为-2价。
显然根据其中《硫代硫酸钠中硫氧化数的实验推证》既然硫代硫酸钠能被氧化为S单质,那么必定反应前存在低于0价的S元素,因此给-2与+6这种观点提供了实验证据支撑。但是我觉得这个逻辑本身有些问题,那就是生成0价S不一定是铁氰化钾氧化导致的,也可以解释为+2价S发生歧化反应所得,但这样S化合价就成了+2价,如果整体分析平均化合价也说得过去。
如何认识硫代硫酸或硫代硫酸根中S的化合价呢?我认为首先应该知道高中阶段的化合价实质就是氧化数。请看下列资料:

《无机化学》主编:张祖德
既然高中阶段的化合价本质上就是氧化数,那么我们就看看氧化数是如何界定的。请看资料:

《无机化学导论》李改仙等编著

《无机化学》主编:张祖德
根据上述资料,如果硫代硫酸作为一个整体分析,其所含S的表观氧化数(平均氧化数)肯定是+2。根据张祖德教授书中所给的连四硫酸根中S的价态分析,根据“静态电负性”那么硫代硫酸中中心S应该为+4价,配位S应该为0价。但是如果照此分析,很多方程式则不好运用氧化还原理论进行分析。例如:

《化学方程式辞典》主编:王希通潘鸿章
上述资料中,方程式①尚且可以用“歧化反应”进行化合价分析,但是这样两个S就都是+2价了。对于反应②如果认为S一部分发生了歧化反应,一部分被Fe3+氧化也可以圆的过去。但是我们知道Fe3+氧化性较强,而硫代硫酸根还原性比较强,例如请看下列资料及反应:

《大学化学实验 I》 何水样等编著

《化学方程式辞典》主编:王希通潘鸿章
既然碘能把硫代硫酸根氧化为+2.5价,三价铁离子氧化性还强于I2。那么硫代硫酸钠与氯化铁产生0价S,解释成歧化所得显然并不合理。最好解释为由-2价氧化而来比较合理。
我们再用软件模拟一下硫代硫酸分子结构及原子所带电荷情况。请看资料:
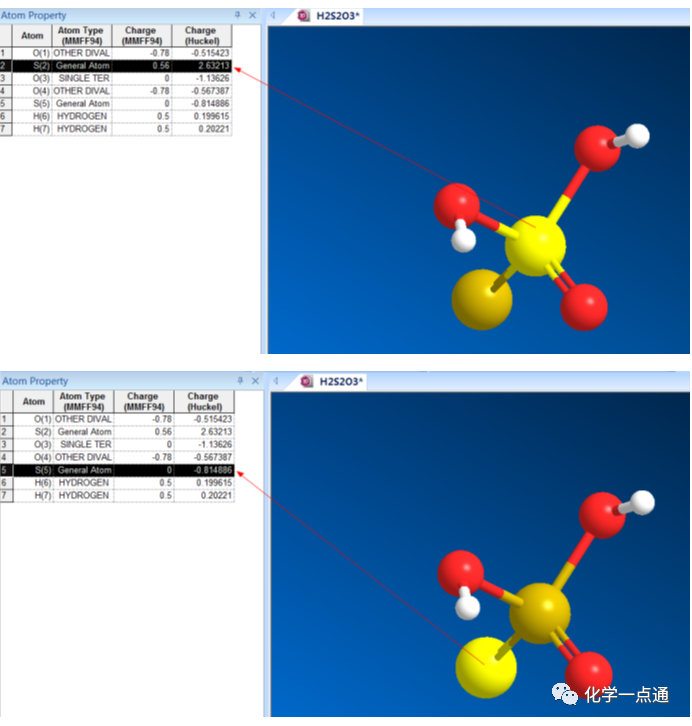
根据软件分析,中心S带正电荷,配位S带负电荷(MMFF94分析电荷为0,Huckel法电荷为-0.815)。据此中心S为+6价,配位S为-2价比较合理。
总结:硫代硫酸或硫代硫酸钠中S的化合价主要有两种观点,一种认为中心S为+4价,配位S为0价,平均化合价(氧化数)为+2;另一种观点认为中心S为+6价,配位S为-2价,平均化合价(氧化数)为+2。氧化数在离子化合物中就是离子所带正负电荷,但在共价化合物中并非原子所带电荷而是一种形式电荷,有很强的人为色彩。氧化数主要用来分析氧化还原反应,很多反应中无论哪种观点都能说得过去,所以通常两种观点到底哪个正确基本没啥鸟用。但有些反应,如FeCl3氧化硫代硫酸钠生成0价的S单质,如果解释为硫代硫酸根歧化而来,那就貌似认可硫代硫酸根氧化性强于Fe3+,同时解释歧化的话那就认为两个S均为+2价而不可能一个+4价一个0价。由于硫代硫酸根还原性很强所以解释歧化与事实不符,因此最好解释为由-2价S被铁离子氧化而来比较合理,另外从软件模拟两种S带电情况看,中心S为+6价,配位S为-2价也是合理的。
———END———
限 时 特 惠: 本站每日持续更新海量各大内部创业教程,永久会员只需98元,全站资源免费下载 点击查看详情
站 长 微 信: yjxmw518




